Gazyva est un nouveau médicament prometteur dans le traitement du lymphome folliculaire au stade avancé jamais traité. Il s’agit d’un type de cancer du sang particulièrement difficile à traiter chaque fois qu’il apparaît chez les patients.
Traiter le lymphome folliculaire (LF de stade II massif)
Le Gazyva permet d’observer de réels progrès dans le traitement du lymphome folliculaire de stade II massif, supérieur à 7 cm, III ou IV jamais traité auparavant. L’étude clinique GALLIUM, qui a permis d’aboutir à un tel constat, a montré une diminution significative du risque de propagation ou de décès chez les patients ayant reçu un schéma à base de Gazyva comparativement à ceux ayant reçu un schéma à base de Rituxian (Rituximab) en traitement initial.
Le lymphome folliculaire (LF) est un type de lymphome non hodgkinien (LNH). C’est une forme indolente (d’évolution lente) et incurable de la maladie qui apparaît lorsque l’organisme produit des lymphocytes B anormaux (globules blancs chargés de lutter contre les infections). C’est le sous-type le plus courant de lymphome indolent.
En 2016, on estime que 2900 Canadiens ont reçu un diagnostic de LF4, une forme incurable de LNH indolent. Cette forme de LNH apparaît généralement chez les personnes de 50 ans et plus et est légèrement plus fréquente chez les femmes que chez les hommes. Lors du diagnostic de LF, il y a généralement des tumeurs dans de nombreuses parties du corps, et le LF peut progresser vers des formes plus agressives de LNH.
Le Gazyva est un médicament de la compagnie de biotechnologie Hoffmann-La Roche limitée (Roche, Canada). Le patronyme de cette structure qui a vu le jour au Canada il y a environ 87 ans est issu de la maison mère Roche, basée à Bâle, en Suisse, spécialisée dans la fabrication de médicaments contre le cancer, les maladies de l’œil et autres maladies infectieuses.
Le Gazyva (Obinutuzumab) a été approuvé par Santé Canada, en association avec une chimiothérapie, suivi en monothérapie chez les maladies.
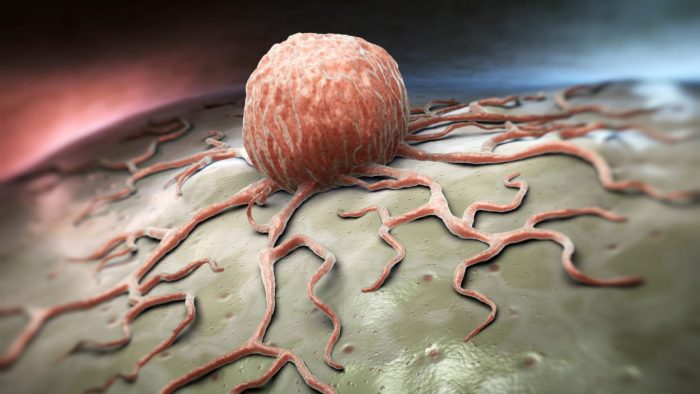
Représentation artistique d’une tumeur cancéreuse Photo : iStock
Quelques données sur l’étude clinique
L’étude a porté sur 1202 patients, dont 138 étaient Canadiens inscrits dans sept sites d’essai clinique dans l’ensemble du pays. Suivant une répartition spécifiée à l’avance, les patients avaient été divisés en plusieurs groupes en fonction de leurs types de lymphomes.
Des patients atteints d’un LF de stade II (massif), III ou IV non traité auparavant ont été répartis aléatoirement selon un rapport de 1:1 pour recevoir GAZVYA ou le rituximab en association avec une chimiothérapie (CHOP, CVP ou bendamustine) suivi de GAZYVA ou du rituximab en monothérapie chez les patients ayant obtenu une réponse complète ou partielle.
Les patients étaient stratifiés en fonction de la chimiothérapie (sélectionnée par chaque site d’essai; tous les patients de ce site recevaient le schéma chimiothérapeutique choisi pendant toute la durée de l’étude), le groupe de risque selon l’indice FLIPI (follicular lymphoma international prognostic index)et la région géographique.
L’étude excluait les patients présentant un LF de grade 3b ou une maladie transformée.
– 83,4 % des patients sous schéma à base de Gazyva et 78,9 % des patients recevant le schéma à base de rituximab ne présentaient pas de progression à 3 ans;
– Taux de réponse complète (RC) de 28% à la fin du traitement d’induction déterminé par tomodensitométrie dans le groupe sous schéma à base de Gazyva comparativement à 27 % dans le groupe sous schéma à base de rituximab;
– Taux de réponse global (RG) de 91% déterminé par tomodensitométrie dans le groupe sous schéma à base de Gazyva comparativement à 88 % dans le groupe sous schéma à base de rituximab.
Source : Hoffmann-La Roche limitée
Lire aussi : Quel est l'état du cancer en 2018? La résistance à certains traitements contre le cancer mieux comprise La propagation des métastases bientôt stoppée? Les métastases mieux comprises Une partie de cache-cache avec le cancer tourne à l’avantage de la science







Pour des raisons indépendantes de notre volonté et, pour une période indéterminée, l'espace des commentaires est fermé. Cependant, nos réseaux sociaux restent ouverts à vos contributions.